L'imitation des conditions physiologiques aide les chercheurs à trouver des liants métalliques
Les chercheurs ont développé une méthode pour identifier les petites molécules qui lient les ions métalliques. Les ions métalliques sont essentiels en biologie. Mais identifier les molécules – et en particulier les petites molécules – avec lesquelles ces ions métalliques interagissent peut s’avérer difficile.
Pour séparer les métabolites à des fins d'analyse, les méthodes métabolomique conventionnelles utilisent des solvants organiques et des pH faibles, ce qui peut provoquer la dissociation des complexes métalliques. Pieter C. Dorrestein de l'Université de Californie à San Diego et ses collègues voulaient conserver les complexes ensemble pour l'analyse en imitant les conditions natives trouvées dans les cellules. Mais s’ils utilisaient des conditions physiologiques lors de la séparation des molécules, ils auraient dû réoptimiser les conditions de séparation pour chaque condition physiologique qu’ils souhaitaient tester.
Au lieu de cela, les chercheurs ont développé une approche en deux étapes qui introduit des conditions physiologiques entre une séparation chromatographique conventionnelle et une analyse spectrométrique de masse (Nat. Chem. 2021, DOI : 10.1038/s41557-021-00803-1). Tout d’abord, ils ont séparé un extrait biologique en utilisant la chromatographie liquide haute performance conventionnelle. Ensuite, ils ont ajusté le pH du flux sortant de la colonne chromatographique pour imiter les conditions physiologiques, ajouté des ions métalliques et analysé le mélange par spectrométrie de masse. Ils ont effectué l’analyse deux fois pour obtenir des spectres de masse de petites molécules avec et sans métaux. Pour identifier quelles molécules lient les métaux, ils ont utilisé une méthode informatique qui utilise les formes des pics pour déduire les connexions entre les spectres des versions liées et non liées.
Selon Dorrestein, une façon d'imiter davantage les conditions physiologiques serait d'ajouter des concentrations élevées d'ions tels que le sodium ou le potassium et de faibles concentrations du métal d'intérêt. « Cela devient une expérience de compétition. En gros, il vous dira : OK, cette molécule dans ces conditions a plus de propension à lier le sodium et le potassium ou ce métal unique que vous avez ajouté », explique Dorrestein. "Nous pouvons infuser simultanément de nombreux métaux différents et nous pouvons vraiment comprendre la préférence et la sélectivité dans ce contexte."
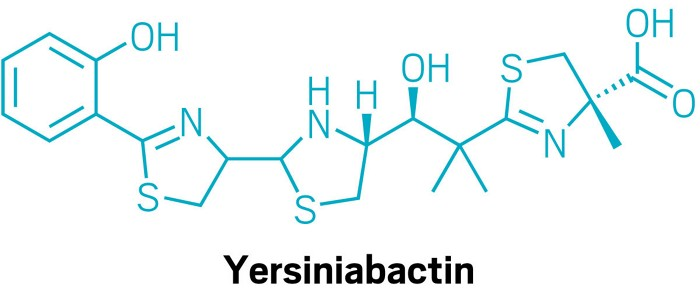
Dans des extraits de culture d’Escherichia coli, les chercheurs ont identifié des composés connus liant le fer, tels que la yersiniabactine et l’aérobactine. Dans le cas de la yersiniabactine, ils ont découvert qu’elle pouvait également lier le zinc.
Les chercheurs ont identifié des composés liant les métaux dans des échantillons aussi complexes que la matière organique dissoute de l’océan. «C'est absolument l'un des échantillons les plus complexes que j'ai jamais examiné», déclare Dorrestein. "C'est probablement aussi complexe, sinon plus, que le pétrole brut." La méthode a identifié l'acide domoïque comme une molécule liant le cuivre et a suggéré qu'il se lie au Cu2+ comme un dimère.
"Une approche omique pour identifier tous les métabolites liant les métaux dans un échantillon est extrêmement utile en raison de l'importance de la chélation biologique des métaux", écrit Oliver Baars, qui étudie les métabolites liant les métaux produits par les plantes et les microbes à l'Université d'État de Caroline du Nord. e-mail.
"Dorrestein et ses collègues fournissent un test élégant et indispensable pour mieux sonder quel pourrait être le rôle physiologique des ions métalliques dans la cellule", écrit Albert JR Heck, pionnier des analyses par spectrométrie de masse native à l'Université d'Utrecht, dans un e-mail. "Une prochaine étape possible serait d'extraire les métabolites dans des conditions natives de la cellule et de les fractionner également dans des conditions natives, pour voir quels métabolites transportent quels ions métalliques cellulaires endogènes."
Actualités Chimie et Ingénierie
ISSN0009-2347
Copyright © 2021 Société américaine de chimie
Heure de publication : 23 décembre 2021

